Vaginal vault reconstruction and apical sling in the treatment of post-hysterectomy prolapsE
- Authors: Shkarupa D.D1, Bezmenko A.A2, Kubin N.D1, Shapovalova E.A1, Pisarev A.V1
-
Affiliations:
- University Clinic of Saint Petersburg State University
- S.M. Kirov Military Medical Academy
- Issue: Vol 66, No 1 (2017)
- Pages: 46-55
- Section: Articles
- URL: https://journals.eco-vector.com/jowd/article/view/6095
- DOI: https://doi.org/10.17816/JOWD66146-55
- ID: 6095
Cite item
Full Text
Abstract
Introduction. Frequency of vaginal vault prolapse (VVP) requiring surgical repair is up to 6-8% and 11.6-45% in patients with prior hysterectomy for uterine prolapse. Reported recurrence rate of VVP following different techniques of surgical correction is up to 10%.
Objective: to evaluate the effectiveness of the novel technique: bilateral sacrospinous fixation of reconstructed vaginal wall (neocervix) by monofilament polypropylene apical sling (Urosling 1; Lintex, Saint Petersburg, Russia) in surgical treatment of VVP.
Methods. This prospective study involved 61 women suffering from post-hysterectomy prolapse. To evaluate the results of surgical treatment, data of a vaginal examination (POP-Q), uroflowmetry, bladder ultrasound, validated questionnaires were used. All listed parameters were determined before the surgery and at control examinations in 1, 6, 12 months after the treatment.
Results. Mean operation time was 35 minutes. No cases of intraoperative damage to the bladder/rectum, as well as clinically significant bleeding were noted. 12-months anatomical cure rate (≤ stage I, POP-Q) was 100%, 94.4% and 100% for apical, anterior and posterior vaginal compartments, respectively. At 1 month of follow-up stress urinary incontinence de novo and urgency de novo were noted in 6.5% and 4.9%, respectively. Statistically significant (p < 0.05) improvement in peak flow rate was observed according to uroflowmetry. Comparison of the scores by the questionnaires revealed a significant improvement in the quality of life in the postoperative period.
Conclusion. Bilateral sacrospinous fixation of reconstructed vaginal wall (neocervix) by monofilament polypropylene apical sling appears to be effective and safe method for treatment patients with vaginal vault prolapse.
Full Text
Введение
По данным В.И. Краснопольского экстирпация матки составляет 38,2 % от общего числа гинекологических операций в РФ [1]. Опубликованы впечатляющие данные о более чем 433 тысячах гистерэктомий, выполненных 2010 г. в США [2]. Одним из распространенных поводов для данного оперативного вмешательства является пролапс тазовых органов (ПТО). При этом данные литературы свидетельствуют о высокой вероятности выпадения купола влагалища в послеоперационном периоде, достигающей 11,6–45 % [3, 4].
Ключевое патогенетическое звено, приводящее к постгистерэктомическому пролапсу тазовых органов (ПГЭ ПТО), заключается в оперативной технике, а именно в отсечении крестцово-маточных и кардинальных связок от парацервикального фиброзного кольца и сводов влагалища. Известно, что указанный связочный комплекс в норме обеспечивает апикальную поддержку структур тазового дна (I уровень по DeLancey). Наиболее часто в лечении ПГЭ ПТО применяются сакровагинопексия, крестцово-остистая фиксация и кольпосуспензия по McCall. Каждая из перечисленных хирургических техник имеет ряд недостатков, не позволяющих использовать ее в качестве универсальной методики, что приводит к необходимости поиска новых подходов к лечению ПГЭ ПТО.
На сегодняшний день одной из наиболее многообещающих технологий является билатеральная крестцово-остистая фиксация, или апикальный слинг, осуществляемая через влагалищный доступ. Данная операция заключается в проведении синтетических сетчатых эндопротезов-лент через крестцово-остистые связки с обеих сторон с последующей их фиксацией к куполу влагалища [5, 6]. В данной методике наиболее уязвимым этапом является присоединение истонченных тканей пролабирующего купола к эндопротезу, что создает технические сложности и может негативно отразиться на результате. Кроме того, известно, что помимо апикального пролапса в 72 % случаев опущения купола влагалища имеют место сопутствующие дефекты тазового дна, такие как цистоцеле, ректоцеле или энтероцеле [7]. По данным, опубликованным DeLancey, частота цисто- и ректоцеле, как проявлений дефекта эндопельвикальной фасции (II уровня поддержки), при постгистерэктомическом пролапсе достигает 67 % [8]. Данное обстоятельство указывает на необходимость одновременной коррекции I и II уровней поддержки для достижения большей эффективности лечения и снижения процента пролапса de novo.
Целью настоящего исследования явилась оценка эффективности новой методики коррекции ПГЭ ПТО, заключающейся в билатеральной крестцово-остистой фиксации реконструированного купола влагалища (так называемый неоцервикс) монофиламентным синтетическим эндопротезом-лентой (апикальный слинг).
Материалы и методы
Данное проспективное нерандомизированное исследование проводилось на базе ФГБУ «СПМЦ» Минздрава России (Университетская клиника СПбГУ). В него вошли женщины с выраженным опущением купола влагалища (III–IV стадий по классификации Baden-Walker), обратившиеся для оперативного лечения в период с сентября 2014 по апрель 2015 г. Критериями исключения были: злокачественные опухоли репродуктивных органов в анамнезе и стрессовое недержание мочи. Все пациентки были информированы о технике операции, рисках и возможных осложнениях. Исследование зарегистрировано и одобрено этическим комитетом клиники, больные подписывали информированное согласие.
Предоперационное обследование включало в себя сбор жалоб, анамнеза жизни и заболевания, физикальное и урогинекологическое обследование. При обнаружении стрессового недержания мочи (жалобы, положительная кашлевая проба) пациентки исключались из исследования. Оценка результатов лечения производилась путем сравнительного анализа данных влагалищного осмотра (POP-Q), урофлоуметрии, УЗИ мочевого пузыря с определением объема остаточной мочи, полученных до оперативного лечения и на контрольных приемах после него. Повторные визиты в послеоперационном периоде осуществлялись на сроках 1, 6 и 12 месяцев, затем ежегодно. Оценка влияния оперативного лечения на качество жизни пациенток производилась путем сравнения баллов по валидизированным опросникам, заполняемым пациентками до вмешательства и через 12 месяцев после него: Pelvic Floor Distress Inventory (PFDI-20), Pelvic Floor Impact Questionnaire (PFIQ-7), Pelvic Organ Prolapse/Urinary Incontinence Sexual Questionnaire (PISQ-12) [9]. Анатомическим рецидивом считалось наличие пролапса в прооперированном компартменте ≥ II стадии (POP Q). Удовлетворенность пациенток произведенным хирургическим вмешательством определялась ответом на вопросы: «Удовлетворены ли Вы результатом лечения? Будете ли Вы рекомендовать данную операцию своим близким?».
Оперативная техника
Предоперационная антибиотикопрофилактика проводилась за час до вмешательства и заключалась во внутривенной инъекции амоксициллина/клавуланата (в соответствии с весом). Операции выполнялись под эндотрахеальной или внутривенной анестезией во всех случаях одними и теми же двумя хирургами, имеющими опыт выполнения данного вмешательства (Д.Д. Шкарупа и Н.Д. Кубин). После глубокой гидропрепаровки стенки влагалища 40 мл 0,9 % раствора натрия хлорида по средней линии производился 5-сантиметровый вертикальный разрез через всю толщу влагалища: слизистую, подслизистый слой и влагалищную фасцию. Разрез выполнялся через ведущую точку пролапса, в качестве которой могли выступать как постгистерэктомический рубец, так и передняя/задняя стенка влагалища. Затем вся толща влагалищной стенки захватывалась в зажимы Эллиса и производилась субфасциальная диссекция паравагинальных тканей тупым путем в направлении сакроспинальных связок с каждой стороны. Установка апикального слинга производилась типично, в соответствии с методикой, опубликованной ранее (рис. 1) [10]. В качестве апикального слинга использовался современный полипропиленовый сетчатый эндопротез I типа — УроСлинг-1 (ООО «Линтекс», Санкт-Петербург). Протез устанавливался при помощи многоразового металлического проводника-иглы Урофикс ПЛ (с облегченной ручкой — «булавка») и одноразового гибкого проводника — туннелера, входящего в комплект с эндопротезом (рис. 2).
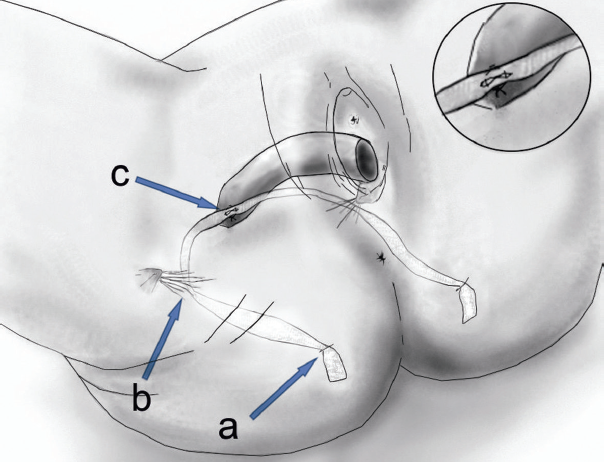
Рис. 1. Схема положения апикального слинга: а — УроСлинг-1, b — крестцово-остистая связка, c — купол влагалища
Fig. 1. The position of the apical sling: а – the tape UroSling 1, b – sacrospinous ligament, c – vaginal cuff
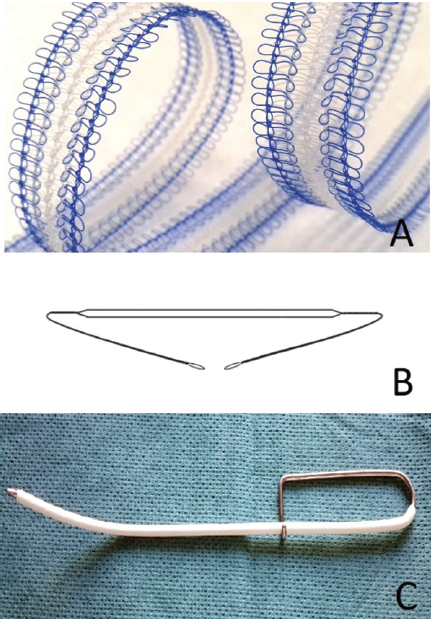
Рис. 2. A, B — эндопротез УроСлинг-1; C — инструмент Урофикс ПЛ с надетым на него тунеллером
Fig. 2. A, B. The tape UroSling 1; C. Urofix PL tool with a tunneler put on
После проведения эндопротеза производилось пальцевое ректальное исследование для проверки целостности прямой кишки и контролировался цвет мочи.
Ключевой момент предлагаемой методики заключается в способе фиксации купола влагалища к эндопротезу. Через центральную часть апикального слинга билатерально проводились две лигатуры из нерассасывающегося материала (Фторекс USP1), используемые в качестве фиксирующих (рис. 3А, а). Затем на внутреннюю поверхность влагалищной (эндопельвикальной) фасции накладывался субфасциальный кисетный шов (ПГА USP1) так, чтобы латеральные стежки проходили над фиксирующими лигатурами слинга, захватывая их в шов (рис. 3А, b). Нить проводилась через всю толщу влагалищной стенки за исключением слизистой. В заключение шов затягивался, создавая конгломерат тканей влагалищной фасции, так называемого неоцервикса (рис. 3В, а). Затем фиксирующие лигатуры слинга завязывались между собой над созданным неоцервиксом (рис. 3В, с). В случае выраженной атрофии влагалищной стенки описанный выше этап формирования неоцервикса повторялся.
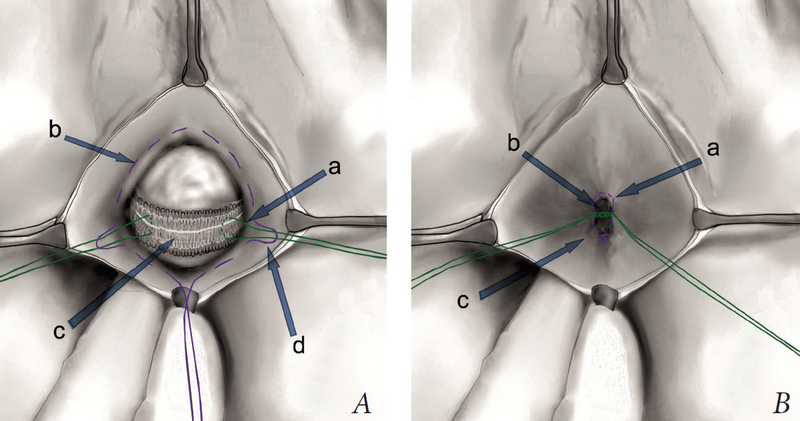
Рис. 3. А — техника наложения субфасциального шва: а — фиксирующие лигатуры апикального слинга, b — кисетный шов на внутренней поверхности фасции, с — УроСлинг-1, d — шов проходит поверх фиксирующих лигатур; В — формирование неоцервикса: а — затянутый кисетный шов, b — лигатуры завязываются между собой над конгломератом тканей, с — неоцервикс
Fig. 3. А. Subfascial colporrhaphy suture technique: a. fixing ligatures of the apical sling, b. purse-string suture on the internal surface of the fascia, c. the tape Urosling 1, d. Purse-string suture passes over; B. Neocervix formation a. the purse-string suture is tied, b. the ligatures are tied above the tissue conglomerate, c. Neocervix
Таким образом, создавалась единая конструкция, состоящая из восстановленной эндопельвикальной фасции и апикального слинга, проведенного через сакроспинальные связки билатерально. Разрез влагалища ушивался рассасывающимся материалом (ПГА USP 2-0). Затем производилось подтягивание эндопротеза за его дистальные концы, и вся конструкция устанавливалась в должной анатомической позиции (рис. 2С). За счет тракции купола влагалища происходило восстановление I уровня поддержки по DeLancey, а предшествующий этап формирования неоцервикса, фиксированного к апикальному слингу, обеспечивал устранение дефекта поддержки II уровня. В обязательном порядке после реконструкции производился контроль просвета прямой кишки — при необходимости выполнялось ослабление натяжения эндопротеза. Дистальные концы имплантата срезались подкожно. Кожные раны ушивались. Осуществлялось тампонирование влагалища салфеткой с левомеколем. Уретральный катетер и тампон удалялись на следующее утро после операции.
Полученные клинические результаты анализировались с использованием программной системы STATISTICA for Windows (версия 10, StatSoft Inc., Tulsa, OK, USA). Для количественных параметров использовался комплекс описательной статистики: средние значения, стандартное отклонение, минимальные и максимальные значения. Обработка шкалы QOL и системы POP-Q производилась путем сопоставления исходных данных и значений, полученных в процессе наблюдения, они сравнивались с помощью парных критериев знаков и Вилкоксона. Анализ частотных характеристик качественных показателей проводился с помощью непараметрических методов c2 и критерия Фишера. Критерием статистической достоверности получаемых выводов мы считали общепринятую в медицинских науках величину p < 0,05.
Результаты
В исследование была включена 61 пациентка со средним возрастом 63,49 ± 8,28 года. Характеристики пациенток представлены в таблице 1. Пролапс тазовых органов послужил причиной предшествующей гистерэктомии у 68,5 % женщин. Ургентное недержание мочи было выявлено у 8 пациенток (13 %).
Таблица 1. Характеристики пациенток
Table 1. Patient characteristics
Показатель | n = 61 |
*Возраст, лет | 63,49 ± 8,28 |
*Индекс массы тела, кг/м2 | 29,35 ± 3,82 |
*Количество родов | 2,03 ± 0,51 |
Постменопауза, n (%) | 52 (85 %) |
Сексуально активные женщины, n (%) | 16 (26,0 %) |
Предшествующие операции, n (%): – гистерэктомия:
– установка субуретрального слинга – передняя/задняя кольпоррафия | 61 (100,0 %) 29 (47,5 %) 32 (52,4 %) 42 (68,5 %) 2 (3,3 %) 9 (14,8 %) |
*Данные представлены в виде средних значений ± стандартное отклонение, s.d | |
Всем пациенткам была произведена реконструкция тазового дна в соответствии с предложенной методикой. Средняя продолжительность операции составила 35 ± 13 минут (25–60), объем интраоперационной кровопотери — 45 ± 15 мл (30–150). Средняя длительность дренирования мочевого пузыря составила 1,05 ± 0,73 дня (максимум 4), длительность пребывания в стационаре — 3,1 ± 0,6 койко-дня (максимум 5). За время проведения исследования не зафиксировано случаев интраоперационного повреждения мочевого пузыря или прямой кишки, равно как и клинически значимого кровотечения, требовавшего переливания компонентов крови. Восемь пациенток в послеоперационном периоде предъявляли жалобы на боли в ягодичной/крестцово-копчиковой области. Данные симптомы были полностью разрешены приемом нестероидных противовоспалительных средств в течение 2 недель. Задержка мочи развилась у 3 (4,9 %) пациенток и разрешилась самостоятельно в течение 5 дней. Основные послеоперационные осложнения представлены в таблице 2.
Таблица 2. Частота послеоперационных осложнений и время их развития
Table 2. Postoperative complications
Осложнения | 1 месяц (n = 61) | 6 месяцев (n = 58) | 12 месяцев (n = 54) |
Гематома в области операции (< 200 мл) | 4 (6,6 %) | 0 | 0 |
Задержка мочи (VОМ > 100 мл) | 3 (4,9 %) | 0 | 0 |
Ургентность de novo | 3 (4,9 %) | 1 (1,7 %) | 1 (1,9 %) |
Стрессовое недержание мочи de novo | 4 (6,6 %) | 1 (1,7 %) | 1 (1,9 %) |
Данные 12-месячного контроля удалось получить у 54 (88,5 %) пациенток. Три женщины отказались от участия в исследовании после первого контрольного осмотра, четыре не явились на годовой визит. Анатомическая эффективность произведенной операции (≤ I стадии пролапса, POP-Q) для купола влагалища (апикальный компартмент) составила 100 % (96,3 % — 0 стадия, 3,7 % — I стадия). Относительно передней влагалищной стенки оперативное лечение оказалось эффективным в 94,4 % (n = 51): у двух пациенток наблюдалось цистоцеле II стадии, а у одной женщины — III стадии. Для заднего компартмента анатомическая эффективность также составила 100 % (табл. 3). Средние значения точек «С», «Ва» и «Вр» изменились с 3,1 ± 2,8 до 7,2 ± 0,3, с 3,0 ± 2,7 до 2,1 ± 0,9 и с 2,9 ± 2,7 до 2,8 ± 0,4 через 12 месяцев после оперативного лечения соответственно (p < 0,001).
Таблица 3.Распределение пациенток в соответствии со стадией пролапса до оперативного лечения и после него
Table 3. Distribution of patients according to preoperative and postoperative prolapse stage
Компартмент | Стадия пролапса (POP-Q) | До лечения n (%) | После лечения n (%) |
Передний | 0 | 0 | 39 (72,1) |
I | 0 | 12 (22,3) | |
II | 5 (9,3) | 2 (3,7) | |
III | 37 (68,5) | 1 (1,9) | |
IV | 12 (22,2) | 0 | |
Апикальный | 0 | 0 | 52 (96,3) |
I | 0 | 2 (3,7) | |
II | 18 (33,3) | 0 | |
III | 30 (55,6) | 0 | |
IV | 6 (11,1) | 0 | |
Задний | 0 | 0 | 46 (85,1) |
I | 0 | 8 (14,9) | |
II | 26 (48,2) | 0 | |
III | 22 (40,7) | 0 | |
IV | 6 (11,1) | 0 |
До реконструкции у 3 женщин (5,6 %) наблюдалось > 100 мл остаточной мочи после мочеиспускания (максимум 250 мл), в послеоперационном периоде этот показатель не превышал 20–30 мл ни у одной пациентки (p < 0,001). Также было выявлено статистически значимое (p < 0,05) увеличение пиковой скорости мочеиспускания (Qmax). Признаки гиперактивности мочевого пузыря, симптоматика, отмеченная до оперативного вмешательства, персистировала у 3 из 8 пациенток (37 %). Ургентность de novo развилась в послеоперационном периоде у 3 (5,6 %) пациенток. В большинстве случаев данная симптоматика была разрешена приемом холинолитиков. Стрессовое недержание мочи de novo было выявлено у 4 (6,5 %) женщин после операции. В течение полугода 3 пациенткам был установлен субуретральный слинг, 1 женщина отказалась от предложенного хирургического лечения ввиду слабой выраженности недержания (см. табл. 2). На протяжении года послеоперационного контроля не было выявлено ни одного случая экструзии эндопротеза. Нарушений со стороны функции прямой кишки (констипация/инконтиненция) также отмечено не было.
Сравнительный анализ данных опросников показал значительное улучшение качества жизни в послеоперационном периоде. Как отражено в таблице 4, суммарные баллы опросников PFDI-20 и PFIQ-7 значимо уменьшились после лечения (p < 0,001). До операции сексуально активными были 16 женщин, 3 из них (18,6 %) предъявляли жалобы на диспареунию, которая у 2 (71,4 %) регрессировала после вмешательства. Диспареуния de novo развилась у 1 пациентки (1,9 %). Согласно данным опросника PISQ-12, качество сексуальной жизни в послеоперационном периоде также значимо улучшилось.
Таблица 4. Оценка качества жизни до и после операции
Table 4. Preoperative and postoperative quality of life data
Опросник | До | После | P-уровень |
PFDI-20 (n = 52) | 101,5 ± 27,2 | 25,1 ± 9,6 | < 0,001 |
PFIQ-7 (n = 51) | 82,7 ± 31,7 | 20,2 ± 8,1 | < 0,001 |
PISQ-12 (n = 16) | 24,7 ± 1,4 | 35,1 ± 0,5 | < 0,001 |
Оценка удовлетворенности пациенток показала, что 98,1 % (53/54) были удовлетворены результатами лечения и 96,3 % (52/54) испытуемых ответили, что они будут рекомендовать данную операцию своим близким.
Дискуссия
Целью реконструктивной хирургии тазового дна является не только восстановление нормальной анатомии и физиологии органов малого таза, но и улучшение качества жизни, в том числе сексуальной. На сегодняшний день описаны разнообразные подходы к коррекции ПГЭ ПТО, как оригинальные, так и их модификации. Наиболее распространенными и изученными являются: сакрокольпопексия (открытым и лапароскопическим доступом), крестцово-остистая фиксация, кульдопластика по McCall. Данные подходы имеют ряд ограничений, таких как длительность операции или высокая стоимость (лапароскопическая/роботическая сакрокольпопексия), а также нередко сопровождаются серьезными интраоперационными (массивная кровопотеря, требующая переливания компонентов крови) и послеоперационными (высокая частота эрозий стенок влагалища, нарушения дефекации, послеоперационный илеус, обструкция мочеточников, диспареуния) осложнениями [11–15, 16]. Люмбосакральный спондилодисцит является одним из специфических осложнений сакрокольпопексии. Данная ятрогенная патология встречается нечасто и описывается зачастую в качестве отдельных случаев, однако требует повторного оперативного вмешательства, отсечения протеза от места фиксации и длительной антибиотикопрофилактики [17]. Очевидным ограничением распространения лапароскопической/роботической сакрокольпопексии являются технические возможности стационара, а также длительность кривой обучения. По сравнению с этими традиционно выполняемыми методиками разработанная нами техника не предполагает использования дорогостоящего оборудования, относительно проста в исполнении, характеризуется незначительной продолжительностью (35 ± 13 минут), низкой частотой интра- и послеоперационных осложнений.
Инфракокцигиальная сакропексия, описанная P. Petros в 1997 г., стала первой методикой, предполагающей коррекцию ПГЭ ПТО вагинальным путем с использованием синтетического материала [18]. Методика была направлена на патогенетическое звено ПГЭ-опущения — восстановление апикального компартмента за счет замещения дефекта крестцово-маточных связок синтетической лентой. В дальнейших публикациях она была переименована в заднюю интравагинальную слингопластику (ЗИВС) [19]. В литературе описаны данные о высокой 9-летней эффективности ЗИВС (93,18 %) с единственным случаем экструзии эндопротеза [20]. Однако эти данные противоречат результатам других исследований, согласно которым частота эрозий находится в пределах 8,5–9,8 % [21, 22]. Причина последней, по всей вероятности, заключается в несовершенной полифиламентной микропористой структуре эндопротеза, используемого при данном оперативном вмешательстве (IVS, Tyco Healthcare).
Идея ЗИВС мигрировала в такие технологии, как Apogee, Elevate (AMS) и Prolift (Ethicon), с единственным отличием — эндопротез (или его части) проходил не в толще параректальной клетчатки, а фиксировался к крестцово-остистым связкам. Однако многочисленные интра- и послеоперационные, а также имплантат-ассоциированные осложнения ограничили широкое распространение данных систем. Отечественными авторами в 2009 г. были опубликованы результаты ретроспективного анализа применения технологии Prolift (Ethicon), выявившие массивное интраоперационное кровотечение, ранения смежных органов, гематомы в послеоперационном периоде, а также mesh-ассоциированные осложнения в 2,9, 3,0, 8,1 и 9,2 % соответственно [23]. В российских источниках описана высокая эффективность (96,4 %) применения системы Elevate (AMS) в коррекции ПГЭ ПТО при сроке наблюдения от 6 месяцев до 2 лет при отсутствии специфических осложнений [24]. Однако в данном исследовании анализируется гетерогенная группа пациентов, которым имплантировались разные типы протеза (передний, задний, их комбинация), а также всем пациенткам выполнялась перинеолеваторопластика.
Эволюция реконструктивной хирургии тазового дна шла по пути уменьшения размеров имплантатов и точек их фиксации, была разработана система UpHold (Boston Scientific). K. Jirschele et al. сообщили о 97 % эффективности использования данной технологии для восстановления апикального и переднего компартментов, однако частота экструзии эндопротеза и повторных оперативных вмешательств в данном исследовании составила 6,52 и 7,53 % соответственно [25]. В 2016 г. были опубликованы данные о 94 % эффективности реконструкции с использованием системы UpHold, однако частота экструзий составила 1,7 %, во всех случаях потребовалось хирургическое вмешательство для коррекции этого осложнения [5]. В этом же исследовании описаны 3 случая перфорации мочевого пузыря и 1 случай интраоперационного кровотечения > 1,000 мл. В нашем исследовании не было ни одного случая имплантат-ассоциированных осложнений, ранения смежных органов, равно как клинически значимого кровотечения.
Недавно были опубликованы результаты вагинальной билатеральной крестцово-остистой фиксации купола влагалища с помощью апикального слинга [6]. Аналогично нашему исследованию авторы использовали монофиламентную полипропиленовую петлю (I-STOP sling, CL Medical, Winchester, MA). Шестимесячная анатомическая (стадия пролапса ≤ I, POP-Q) и субъективная эффективность составила 100 и 78,7 % соответственно. Однако авторами описаны 1 случай кровопотери, потребовавшей гемотрансфузии, и 2 случая (4,3 %) экструзии шовного материала.
В отличие от вышеприведенных публикаций, в нашем исследовании не было выявлено ни одного случая экструзии эндопротеза как в результате использования современного сетчатого материала, так и благодаря уникальному способу фиксации купола влагалища к нему. Основное преимущество предлагаемой техники заключается в отсутствии прямого контакта слинга и его фиксирующих лигатур с влагалищной стенкой. Образованный с помощью кисетного шва неоцервикс используется в качестве опорной структуры для фиксации свода влагалища к эндопротезу.
Зачастую при ПГЭ ПТО имеют место сопутствующие дефекты эндопельвикальной фасции, что вынуждает хирургов дополнять апикальную коррекцию восстановлением передней/задней влагалищной стенки. Однако традиционно выполняемая кольпоррафия сопровождается высокой частотой рецидивов, достигающей в случае коррекции цистоцеле, по данным некоторых авторов, 70 % [26]. Описано исследование, результаты которого свидетельствуют о низкой эффективности передней кольпоррафии как превентивного метода в отношении цистоцеле de novo после крестцово-остистой фиксации [27]. Последнее может быть объяснено техникой традиционной кольпоррафии, заключающейся в наложении отдельных рассасывающихся швов на наружную поверхность влагалищной фасции. Предлагаемая нами техника реконструкции купола влагалища предполагает наложение непрерывного шва на внутреннюю поверхность фасции, благодаря чему данный шовный материал изолируется от слизистой влагалища, что позволяет использовать нерассасывающиеся нити при достаточной толщине фасции, повышая тем самым прочность.
Обобщая вышесказанное, можно констатировать, что хороший анатомический результат во всех трех компартментах, полученный в нашем исследовании, был достигнут благодаря созданию единой конструкции, состоящей из неоцервикса (конгломерата из тканей из восстановленной эндопельвикальной фасции и других структур стенки влагалища), фиксированного к синтетичеcкому апикальному слингу. Описанная методика обладает всеми преимуществами нативной пластики (минимальные риски для пациентки) и надежностью реконструкции тазового дна с использованием синтетического материала. Она характеризуется непродолжительным временем операции, малым количеством койко-дней, низкой частотой интра- и послеоперационных осложнений.
Однако, учитывая короткий период наблюдения (12 месяцев), трудно прогнозировать долгосрочные результаты использования данной методики, что требует дальнейшего наблюдения.
Заключение
Билатеральная крестцово-остистая фиксация вагинальным доступом с применением современного монофиламентного синтетического эндопротеза-ленты (апикального слинга) в сочетании с реконструкцией купола влагалища (формированием неоцервикса) может применяться с высокой эффективностью и безопасностью для коррекции постгистерэктомического пролапса тазовых органов.
About the authors
Dmitry D Shkarupa
University Clinic of Saint Petersburg State University
Author for correspondence.
Email: shkarupa.dmitry@mail.ru
Ph.D., Deputy Director for medical care, Chief Urologist Russian Federation
Alexandr A Bezmenko
S.M. Kirov Military Medical Academy
Email: bezmenko@yandex.ru
Ph.D., Obstetrician-gynecologist of the Department of Obsterics and Gynecology, Assistant of the Department of Obsterics and Gynecology Russian Federation
Nikita D Kubin
University Clinic of Saint Petersburg State University
Email: nikitakubin@gmail.com
Ph.D., Urologist of the Department of Urology Russian Federation
Ekaterina A Shapovalova
University Clinic of Saint Petersburg State University
Email: Katerina_andmed@mail.ru
Obstetrician-gynecologist of the Gynecology Department Russian Federation
Alexey V Pisarev
University Clinic of Saint Petersburg State University
Email: alexey.v.pisarev@gmail.com
Urologist of the Department of Urology Russian Federation
References
- Краснопольский В.И., Буянова С.Н., Щукина Н.А., Попов А.А. Оперативная гинекология. – М.: МЕДпресс-информ, 2010. [Krasnopol’skiy VI, Buyanova SN, Shchukina NA, Popov AA. Operativnaya ginekologiya. Moscow: MEDpress-inform; 2010. (In Russ.)]
- Wright JD, Herzog TJ, Tsui J, et al. Nationwide trends in the performance of inpatient hysterectomy in the United States. Obstet Gynecol. 2013122(2 Pt 1):233-41. doi: 10.1097/AOG.0b013e318299a6cf.
- Nyyssönen V, Tanvensaari-Matilla A, Santala M. Posterior intravaginal slingplasty versus unilateral sacrospinous ligament fixation in treatment of vaginal vault prolapse. ISRN Obstet Gynecol. 2013. doi: 10.1155/2013/958670.
- Flynn BJ, Webster GD. Surgical management of the apical vaginal defect. Curr Opinion Urol. 2002;12(4):353-8.
- Altman D, Mikkola TS, Bek KM, et al. Pelvic organ prolapse repair using Upholdä Vaginal Support System: a 1-year multicenter study. Int Urogynecol J. 2016;27:1337-45. doi: 10.1007/s00192-016-2973-0.
- Alas AN, Pereira I, Chandrasekaran N, et al. Apical sling: an approach to posthysterectomy vault prolapse. Int Urogynecol J. 2016;27(9):1433-36. doi: 10.1007/s00192-016-3010-z.
- Uzoma A, Farag KA. Vaginal vault prolapse. Obstet Gynecol Int. 2009. doi: 10.1155/2009/275621.
- DeLancey JO. Anatomic aspects of vaginal eversion after hysterectomy. Am J Obstet Gynecol. 1992;166:1717-24.
- Шкарупа Д.Д., Кубин Н.Д., Пешков Н.О., и др. Русскоязычные версии опросников для оценки качества жизни больных с пролапсом тазовых органов и стрессовым недержанием мочи // Экспериментальная и клиническая урология. – 2016. – № 1. – С. 94–97. [Shkarupa DD, Kubin ND, Peshkov NO, et al. Russkojazychnye versii oprosnikov dlja ocenki kachestva zhizni bol’nyh s prolapsom tazovyh organov i stressovym nederzhaniem mochi. Jeksperimental’naja i klinicheskaja urologija. 2016;(1):94-97. (In Russ.)]
- Шкарупа Д.Д., Кубин Н.Д., Шаповалова Е.А., и др. Комбинированная реконструкция тазового дна при дефектах I и II уровней поддержки: задний интравагинальный слинг и субфасциальная кольпоррафия // Акушерство и гинекология. – 2016. – № 8. – C. 99–105. [Shkarupa DD, Kubin ND, Shapovalova EA, et al. Combined pelvic floor repair in Levels I and II support defects: Posterior intravaginal sling and subfascial colporrhaphy. Obstetrics and Gynecology. 2016;(8):99-105. (In Russ.)]
- Maher CF, Qatawneh AM, Dwyer PL, et al. Abdominal sacral colpopexy or vaginal sacrospinous colpopexy for vaginal vault prolapse: a prospective randomized study. Am J Obstet Gynecol. 2004 Jan;190(1):20-6. doi: 10.1016/j.ajog.2003.08.031.
- Holley RL, Varner RE, Gleason BP, et al. Sexual function after sacrospinous ligament fixation for vaginal vault prolapse. J Reprod Med. 1996;41:355-358.
- Choi KH, Hong JY. Management of pelvic organ prolapse. Korean Journal of Urology. 2014;55:693-702. doi: org/10.4111/kju.2014.55.11.693.
- Margulies RU, Rogers MA, Morgan DM. Outcomes of transvaginal uterosacral ligament suspension: systematic review and metaanalysis. Am J Obstet Gynecol. 2010;202:124-34. doi: 10.1016/j.ajog.2009.07.052.
- Siff LN, Barber MD. Native tissue prolapse repairs: comparative effectiveness trials. Obstet Gynecol Clinics of N Am. 2016;43(1):69-81. doi: 10.1016/j.ogc.2015.10.003.
- Атрошенко К.В. Лапароскопическая и робот-ассистированная сакрокольпопексия: показания, техника, отдаленные результаты: автореф. дис. … канд. мед. наук. – М., 2016. [Atroshenko KV. Laparoskopicheskaja i robot-assistirovannaja sakrokol’popeksija: pokazanija, tehnika, otdalennye rezul’taty. [dissertation] Moscow; 2016. (In Russ.)]
- Попов A.A., Мананникова Т.Н., Рамазанов М.Р., и др. Лапароскопическая сакрокольпопексия и операция Prolift в хирургии генитального пролапса // Журнал акушерства и женских болезней. – 2009. – № 5. – C. M39. [Popov AA, Manannikova TN, Ramazanov MR, et al. Laparoskopicheskaja sakrokol’popeksija i operacija Prolift v hirurgii genital’nogo prolapsa. Journal of Obstetrics and Women’s Diseases. 2009;(5):M39. (In Russ.)]
- Petros PE. New ambulatory surgical methods using an anatomical classification of urinary dysfunction improve stress, urge, and abnormal emptying classification of urinary dysfunction. Int Urogynecol J. 1997;8:270-8.
- Farnsworth BN. Posterior intravaginal slingplasty (infracoccygeal sacropexy) for severe posthysterectomy vaginal vault prolapsed – a preliminary report on efficacy and safety. Int Urogynecol J Pelvic Floor Dysfunct. 2002;13:4-8.
- Capobianco G, Donolo E, Wenger JM. Efficacy and 9 years’ follow-up of posterior intravaginal slingplasty for genital prolapse. J Obstet Gynaecol Res. 2014;40(1):219-23. doi: 10.1111/jog.12162.
- Cosma S, Preti M, Mitidieri M, et al. Posterior intravaginal slingplasty: efficacy and complications in a continuous series of 118 cases. Int Uroginecol J. 2011;22(5):611-619. doi: 10.1007/s00192-010-1350-7.
- Chen HY, Ho M, Chang YY, et al. Risk factors for surgical failure after posterior intravaginal slingplasty: a case series. Eur J Obstet Gynecol Reprod Biol. 2011;155(1):106-109. doi: 10.1016/j.ejogrb.2010.12.005.
- Попов A.A., Мананникова Т.Н., Мачанските О.В., и др. Осложнения экстраперитонеальной кольпопексии (PROLIFT) // Журнал акушерства и женских болезней. – 2009. – № 5. – C. M40. [Popov AA, Manannikova TN, Machanskite OV, et al. Oslozhnenija jekstraperitoneal’noj kol’popeksii (PROLIFT). Journal of Obstetrics and Women’s Diseases. 2009;(5):M40. (In Russ.)]
- Макаров О.В., Камоева С.В., Голубева Д.В. Трансвагинальная система Элевейт (Elevate) в реконструктивной хирургии тазового дна после гистерэктомии // Медицинский альманах. – 2011. – Т. 19. – № 6. – C. 142–144. [Makarov OV, Kamoeva SV, Golubeva DV. Transvaginal’naja sistema Jelevejt (Elevate) v rekonstruktivnoj hirurgii tazovogo dna posle gisterjektomii. Medicinskij al’manah. 2011;19(6):142-144. (In Russ.)]
- Jirschele K, Seitz M, Zhou Y, et al. A multicenter, prospective trial to evaluate mesh – augmented sacrospinous hysteropexy for uterovaginal prolapse. Int Urogynecol J. 2015;26:743-8. doi: 10.1007/s00192-014-2564-x.
- Weber AM, Walters MD, Piedmonte MR, et al. Anterior colporrhaphy: a randomized trial of three surgical techniques. Am J Obstet Gynecol. 2001;185:1299-1304.
- De Castro EB, Juliato CR, Piedemonte LA, et al. Impact of sacrospinous colpopexy associated with anterior colporrhaphy for the treatment of dome prolapse on all three vaginal compartments. Rev Bras Gynecol Obstet. 2016;38(2):77-81. doi: 10.1055/s-0035-1571264.
Supplementary files








