Assotiation of total carotenoid level in maize grain (Zea mays L.) with polimorphic site InDel1 in PSY1 gene
- Authors: Orlovskaya O.A.1, Vakula S.I.1, Khotyleva L.V.1, Kilchevsky A.V.2
-
Affiliations:
- Institute of Genetics and Cytology of the National Academy of Sciences of Belarus
- National Academy of Sciences of Belarus
- Issue: Vol 14, No 3 (2016)
- Pages: 28-34
- Section: Articles
- URL: https://journals.eco-vector.com/ecolgenet/article/view/5480
- DOI: https://doi.org/10.17816/ecogen14328-34
- ID: 5480
Cite item
Full Text
Abstract
Background. The Maize is the only major cereal crop that can naturally accumulate appreciable levels of carotenoids which are the source of provitamin A. The estimation of assotiation of total carotenoid level in maize grain with polimorphism PSY1 InDel1 was made.
Materials and Methods. We used collection of 54 maize genotypes of different eco-geographical origin, methods of PCR analysis, spectrophotometry, statistical analysis in this study.
Results. Total carotenoid content of genotypes with favorable allele of InDel1 was 0,60 mg/100 g, which was significantly higher than that of the samples with unfavorable allele (0,43 mg/100 g).
Conclusion. Thus, the use of PCR-based markers for the PSY1 InDel1 polymorphism is a reliable method for the identification of genotypes with high carotenoid accumulation in maize grain.Keywords
Full Text
ВВЕДЕНИЕ
Витамин А необходим для развития и нормального функционирования зрительной, иммунной и половой систем, поддержания целостности эпителиальных тканей [9]. По данным Всемирной организации здравоохранения, витамин А является одним из наиболее дефицитных витаминов, необходимых для жизнедеятельности человека [4]. Однако в организме человека он не синтезируется и, следовательно, должен поступать с пищей. Кукуруза — единственная из основных зерновых культур, способная накапливать значительное количество каротиноидов, которые, являясь предшественниками провитамина А (про-А) и антиоксидантами, обеспечивают защиту от рака и ряда хронических заболеваний [5]. Про-А включает в себя β- и α-каротин, β-криптоксантин, которые в результате окислительного расщепления могут быть преобразованы в витамин А. Тем не менее содержание про-А обычно составляет только 10–20 % от общего объема каротиноидов зерна кукурузы, в то время как содержание лютеина и зеаксантина достигает 45 и 35 % соответственно [3]. Концентрацию данного провитамина можно повысить селекционным путем, используя природную генетическую изменчивость уровня каротиноидов в зерне кукурузы. Одной из основных проблем селекции кукурузы с высоким уровнем накопления про-А является значительная стоимость анализа содержания компонентов каротиноидов в зерне методом высокоэффективной жидкостной хроматографии (ВЭЖХ). Маркер-сопутствующая селекция, используя недорогие ДНК-маркеры, тесно сцепленные с целевыми локусами, может помочь в ее решении. Последние достижения в области молекулярной биологии позволили выявить ключевые гены, участвующие в регуляции биосинтеза каротиноидов. Установлено, что у кукурузы решающую роль в накоплении про-А играют три гена — PSY1, LcyE и СrtRB1 [6]. Фермент фитоенсинтаза (кодируется геном PSY1) катализирует первый этап биосинтеза, ведущий к образованию фитоена из геранилгеранилпирофосфата. Следующим ключевым этапом является циклизация ликопина. Ликопин-ε-циклаза (LCYE) и/или ликопин-β-циклаза (LCYВ) замыкает молекулу ликопина в кольцо, формируя молекулы α-каротина и β-каротина. β-каротингидроксилаза (СRTRB) катализирует превращение α-каротина и β-каротина в зеаксантин/лютеин и β-криптоксантин/зеаксантин соответственно. Гены PSY1, LcyE и CrtRB1 по-разному влияют на содержание про-А. Высокий уровень естественной изменчивости компонентов про-А во многом связан с повышением активности PSY1 [6] и со снижением экспрессии LcyE и CrtRB1 [4], что соответствует биологическим функциям этих генов. Сочетание благоприятных аллелей LcyE и CrtRB1 увеличивает содержание β-каротина за счет других компонентов каротиноидов, в то время как PSY1 может повысить содержание β-каротина за счет роста количества субстрата, вступающего в биосинтез каротиноидов.
В эндосперме белосемянной кукурузы уровень содержания каротиноидов очень низок, но сверхэкспрессия в белом зерне гена PSY1 приводит к существенному увеличению содержания каротиноидов, что подтверждает важную роль PSY1 в их биосинтезе у кукурузы [14]. В результате изучения структуры гена PSY1 найдено четыре главных полиморфизма (InDel1, 378 bp; InDel2, 644 bp; InDel4, 390 bp; SSR7, CCA тринуклеотидный повтор) в 5’-UTR-области, и два полиморфизма (InDel8, 345 bp и InDel9, 18 bp) выявлены в 3’-UTR. Кроме того, были определены три SNP, вызывающие аминокислотные замены: SNP3 (Thr на Ser), SNP5 (Gly на Arg) и SNP7 (Thr на Asn) [7]. Разработаны ДНК-маркеры к пяти InDels, одному SSR и трем SNPs [13], которые были использованы для проверки их ассоциации с общим содержанием каротиноидов и их отдельных компонентов на большой популяции из 527 линий кукурузы. Установлено, что с общим уровнем каротиноидов достоверно коррелировали только InDel1 и SNP7 [6].
Целью нашего исследования было оценить ассоциацию уровня содержания каротиноидов в зерне кукурузы с аллельным полиморфизмом сайта InDel1 гена PSY1 в коллекции образцов кукурузы различного эколого-географического происхождения.
МАТЕРИАЛЫ И МЕТОДЫ
В исследовании использовалась коллекция из 54 генотипов кукурузы различного эколого-географического происхождения, включающая 20 самоопыленных линий селекции РНДУП «Полесский институт растениеводства» (Гомельская обл., Беларусь), 10 самоопыленных линий из ГНУ «Всероссийский НИИ кукурузы» (г. Пятигорск, Россия), 22 образца селекции России, Молдовы, Украины, Италии, Венгрии, США и других стран из коллекции ГНУ «Всероссийский институт растениеводства» (г. Санкт-Петербург, Россия), 2 образца из Maize Genetics Cooperation Stock Center (USA).
Выделение ДНК осуществляли из зерна при помощи набора реагентов Genomic DNA Purification Kit (Thermo Scientific) согласно инструкции производителя. Использовали следующие последовательности праймеров, специфичные к PSY1 InDel1: F: AGACATCACACACACACGACAC
и R: GTAACTCACCAGGCTCACTTGT [6].
Полимеразную цепную реакцию проводили в реакционной смеси объемом 15 мл, содержащей: 0,2 мМ каждого dNTP, по 10 пM прямого и обратного праймеров, 7,5 нг ДНК, 0,2 ед. Taq-полимеразы в 2× буфере, содержащем 6 мМ MgCl2. Также в буфер входил желтый краситель, облегчающий нанесение пробы после ПЦР на гель. Краситель мигрирует ниже фрагментов длиной 20 н. п., что позволяет вести электрофорез до его полной элиминации из геля. Для амплификации использована следующая программа: предварительная денатурация 15 мин при 95 °C; 35 циклов, включающих: 1 минуту при 99 °C, 15 с при 68 °C, 30 с при 72 °C; финальная элонгация 2 мин при 72 °C.
Продукты ПЦР-реакции разделяли в 1,5 % агарозном геле в 1× TAE буфере. Визуализацию продуктов ПЦР-анализа проводили при помощи системы для документирования электрофореграмм Bio-Print (Vilber Lourmat). Размеры амплифицированных фрагментов определяли относительно маркера GeneRuler 100bp DNA Ladder Plus (Thermo Scientific).
Анализ общего содержания каротиноидов в зерне образцов кукурузы проводился согласно Руководству по методам контроля качества и безопасности биологически активных добавок к пище [1] в лабораторно-аналитическом центре оценки качества новых сортов и гибридов овощных культур при хранении и переработке Всероссийского НИИ селекции и семеноводства овощных культур (Московская обл., Россия).
Для статистической обработки данных использовали программный пакет Statistica 10.0 для Windows.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Китайскими учеными проведен анализ ассоциаций между семью информативными сайтами гена PSY1 и содержанием основных компонентов каротиноидов (лютеина, зеаксантина, β-криптоксантина, β-каротина, общих каротиноидов, про-А). Наиболее высокие ассоциации были установлены между содержанием общих каротиноидов и полиморфизмами InDel1 и SNP7 (p = 7,78Е–04 и 0,0044 соответственно). Показано, что данные полиморфизмы также связаны с уровнем содержания других пяти каротиноидов. Однако значимость их влияния на проявление этих показателей варьировала в зависимости от сезона проведения эксперимента, что, возможно, обусловлено эффектами среды [6]. Нами изучен полиморфизм сайта InDel1 гена PSY1в коллекции 54 образцов кукурузы различного происхождения. Благоприятный аллель 0 — делеция 378 п. н. (размер аллеля 870 п. н.) выявлен у 40 генотипов из 54 изученных нами. Делеция 378 п. н. встречалась с высокой частотой у большинства линий селекции РНДУП «Полесский институт растениеводства» (95 %) (рис. 1) и ГНУ «Всероссийский НИИ кукурузы» (80 %). В коллекции ВИРа генотипов с благоприятным аллелем обнаружено меньше — 59,1 %.
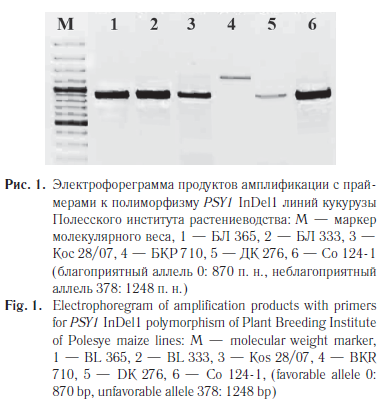
Согласно данным литературы благоприятный аллель 0 сайта InDel1 встречается с высокой частотой у образцов желтосемянной кукурузы. Так, в коллекции из 278 линий кукурузы тропического/субтропического происхождения данный аллель обнаружен у 100 % генотипов, а в коллекции из 226 линий, адаптированных к условиям умеренного климата, — у 92 % [6]. Следует отметить, что в генофонде тропических линий кукурузы данный аллель встречается чаще, чем у линий, культивируемых в регионах умеренного климата, что указывает на потенциал увеличения общего содержания каротиноидов в зерне кукурузы данных генотипов.
На основании визуальной оценки определяли окраску зерна кукурузы по следующей шкале: светло-желтая, желтая, светло-оранжевая, оранжевая, оранжево-коричневая, красная. У 22 из 54 образцов кукурузы с различной окраской зерна методом спектрофотометрии было оценено общее содержание каротиноидов (табл. 1). Выявлены значительные различия по данному показателю у исследованных генотипов (0,21–1,16 мг/100 г). Наиболее высокая концентрация каротиноидов отмечена для линий белорусской селекции — Со 124–1, БЛ 990, МСП 1984/00 (более 1 мг/100 г). Высокая значимость влияния генотипа на уровень накопления каротиноидов в зерне кукурузы подтверждена результатами дисперсионного анализа (табл. 2). Общий уровень изменчивости по данному признаку составил 48,68 % (межгрупповая дисперсия 0,07), вариация внутри образца значительно ниже и не превышает 5,48 % (внутригрупповая дисперсия от 1,1 × 10–4 до 3,3 × 10–3).
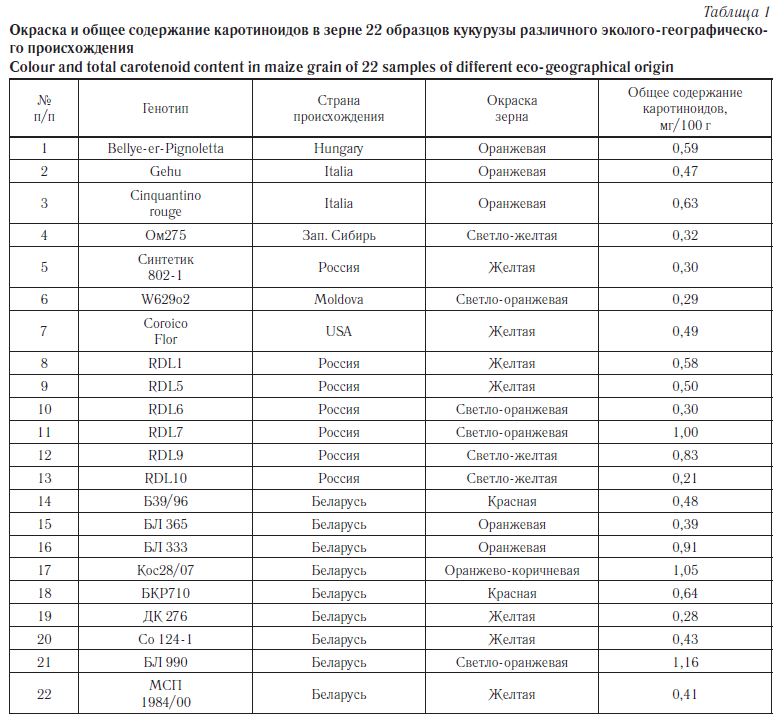

Полученные результаты согласуются с литературными данными. Так, в работе американских ученых проведена оценка фенотипической изменчивости содержания девяти каротиноидов в зерне 201 инбредной линии кукурузы [11]. Установленные высокие значения наследуемости данного признака для подавляющего большинства изученных каротиноидов позволяют предположить, что их изменчивость в значительной степени определяется генетическими, а не средовыми факторами. В данном исследовании выявлена высокая наследуемость уровня содержания основных компонентов про-А — β-каротина и β-криптоксантина (0,82 и 0,95 соответственно), что указывает на эффективность селекционного отбора генотипов кукурузы с высоким содержанием про-А. Fu et al., проводя количественный анализ каротиноидов у 129 линий кукурузы, адаптированных к условиям умеренного климата, выявили широкий диапазон изменчивости по признаку «содержание общих каротиноидов» (1,09–31,89 мг/г) и высокое значение наследуемости признака — 0,91, что свидетельствует о генетической обусловленности фенотипических различий данных линий кукурузы по этому признаку [6].
Согласно проведенному анализу установлено, что общее количество каротиноидов, накапливаемых в эндосперме семян, возрастает в ряду окраски: желтые < светло-желтые < красные < оранжевые < светло-оранжевые < оранжево-коричневые (табл. 3). Для оценки связи градаций окраски кукурузного зерна и содержания в них каротиноидов мы использовали непараметрический корреляционный анализ Спирмана. Выявлено, что связь между признаками слабая, недостоверная (коэффициент корреляции r = 0,23, коэффициент детерминации R2 = 0,05), что не позволяет отбирать образцы кукурузы с высоким уровнем каротиноидов на основании только визуальной оценки окраски зерна (рис. 2).
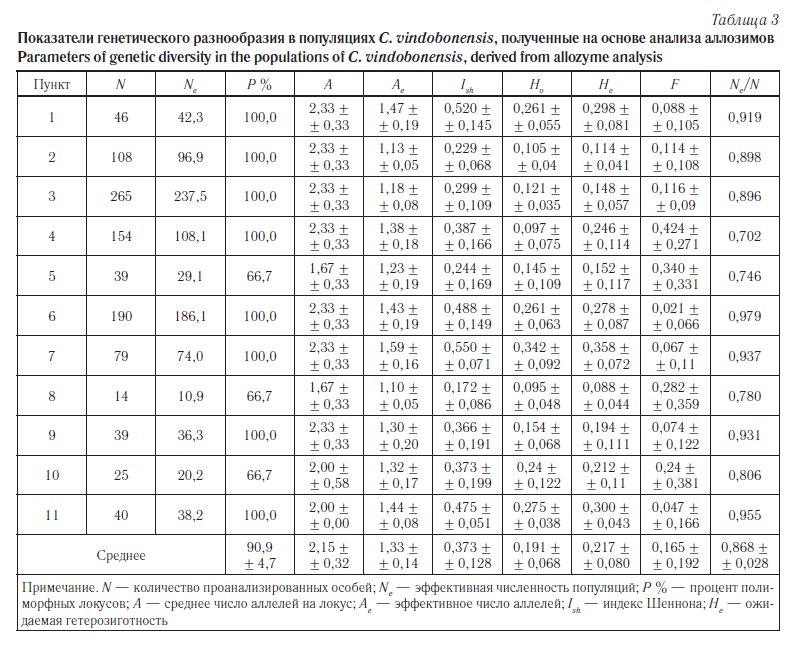

В литературе встречаются противоречивые данные о связи уровня содержания каротиноидов с окраской зерна кукурузы. В одних работах представлены результаты, согласно которым слабая корреляция выявлена между окраской зерна и общим содержанием каротиноидов (R2 = 0,18) и содержанием β-каротина (R2 = 0,03) [12], в других, напротив, показано, что более насыщенный цвет зерна связан как с более высоким накоплением общих каротиноидов, так и про-А каротиноидов [2]. Большинство авторов склоняются к мнению, что у кукурузы различия в интенсивности окраски зерна могут быть связаны с уровнем содержания общих каротиноидов, но не с концентрацией провитамина-А [8, 10].
Так как отбор генотипов кукурузы с высокой концентрацией каротиноидов в зерне на основе его окраски не надежен, нами проведен анализ содержания каротиноидов в зерне образцов кукурузы, различающихся аллельным составом полиморфизма PSY1 InDel1. Показано, что в эндосперме генотипов, несущих благоприятный аллель InDel1-0, содержание каротиноидов в среднем составило 0,60 мг/100 г, что согласно результатам t-теста Стьюдента (t = 2,44, достоверно при α ≤ 0,05) достоверно выше содержания каротиноидов, показанных для образцов с неблагоприятным аллелем 378 (0,43 мг/100 г).
Коэффициент корреляции Спирмана между общим содержанием каротиноидов в зерне и аллельным состоянием полиморфизма PSY1 InDel1 статистически значим (при α ≤ 0,05) и составляет 0,33 (рис. 3), что подтверждает достоверную ассоциацию уровня накопления каротиноидов в зерне кукурузы с аллельным полиморфизмом сайта InDel1 гена PSY1.
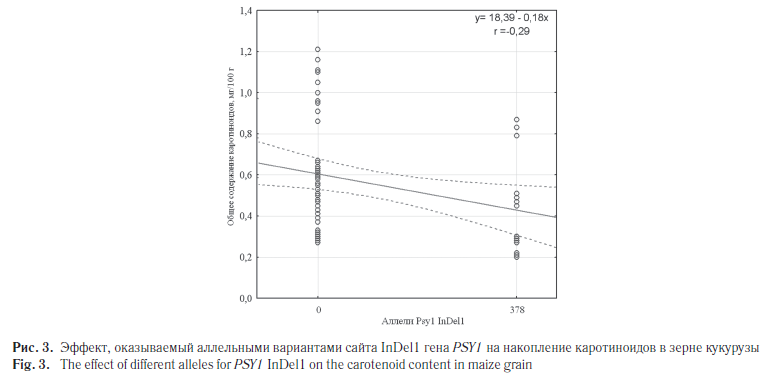
Известно, что кроме гена PSY1 существенный вклад в изменчивость уровня содержания каротиноидов вносят гены LcyE и СrtRB1. При отборе генотипов с благоприятными аллелями полиморфных сайтов гена LcyE происходит перераспределение ликопина в сторону синтеза семейства β-каротиноидов, а отбор благоприятных аллелей полиморфизмов гена СrtRB1 снижает степень конверсии β-каротиноидов в другие метаболиты, тем самым увеличивая концентрацию β-каротина и про-А в зерне кукурузы [3, 4]. Необходимо подчеркнуть важную роль гена PSY1не только в увеличении общего содержания каротиноидов, но и в накоплении β-каротина и провитамина А. Например, некоторые образцы кукурузы, несмотря на наличие благоприятных аллелей полиморфных сайтов СrtRB1, характеризуются низким содержанием β-каротина и про-А. Кроме того, для данных генотипов отмечается низкое содержание общих каротиноидов [3]. Данный факт позволяет предположить, что для реализации потенциала благоприятных аллелей гена СrtRB1 необходимым условием является высокий уровень содержания общих каротиноидов. Таким образом, знание путей биосинтеза каротиноидов в зерне кукурузы и ключевых генов, регулирующих каждый их этап, помогает создавать генотипы с высоким содержанием нужных компонентов.
ЗАКЛЮЧЕНИЕ
В результате изучения полиморфизма сайта InDel1 гена PSY1 у 40 генотипов из 54 изученных нами образцов кукурузы различного эколого-географического происхождения выявлен благоприятный аллель 0, который ассоциирован с высоким уровнем содержания общих каротиноидов. Показано, что эффективность визуального отбора высококаротиноидных линий кукурузы ограничена отсутствием достоверной зависимости между окраской зерна и уровнем накопления каротиноидов. С помощью корреляционного анализа Спирмана установлена значимая ассоциация концентрации каротиноидов в зерне с аллельным полиморфизмом PSY1 InDel1. В связи с вышеизложенным использование молекулярно-генетического скрининга по функциональным маркерам к полиморфизму Psy1 InDel1 является более точным и надежным методом идентификации перспективных генотипов кукурузы с высоким содержанием общих каротиноидов в зерне.
БЛАГОДАРНОСТИ
Авторы выражают благодарность д-ру биол. наук С.М. Надежкину и д-ру с.-х. наук Н.А. Голубкиной (ВНИИССОК, Россия) за оценку уровня общего содержания каротиноидов в зерне 22 образцов кукурузы.
Авторы заявляют об отсутствии конфликта интересов.
About the authors
Olga A. Orlovskaya
Institute of Genetics and Cytology of the National Academy of Sciences of Belarus
Author for correspondence.
Email: O.Orlovskaya@igc.by
Leading researcher, laboratory of ecological genetics and biotechnology Russian Federation
Svetlana I. Vakula
Institute of Genetics and Cytology of the National Academy of Sciences of Belarus
Email: svettera@yandex.ru
Junior researcher, laboratory of ecological genetics and biotechnology Russian Federation
Lubov V. Khotyleva
Institute of Genetics and Cytology of the National Academy of Sciences of Belarus
Email: L.Khotyleva@igc.by
Main researcher, laboratory of ecological genetics and biotechnology Russian Federation
Alexander V. Kilchevsky
National Academy of Sciences of Belarus
Email: Kilchev@presidium.bas-net.by
Main scientific secretary Russian Federation
References
- Руководство по методам контроля качества и безопасности биологически активных добавок к пище. — М.: Федеральный центр госсанэпиднадзора Минздрава России, 2004. — 240 с. [Rukovodstvo po metodam kontrolya kachestva i bezopasnosti biologicheski ak tivnykh dobavok k pishche. Moscow: Federal’nyi tsentr gossanepidnadzora Minzdrava Rossii; 2004. P. 240 (In Russ.)]
- de Almelda Rios S, Paes MCD, Cardoso WS, et al. Colour of corn grains and carotenoid profile of importance for human health. American Journal of Plant Science. 2014;5:857-862. doi: 10.4236/aips.2014.56099.
- Azmach G, Gedil M, Menkir F, et al. Marker-trait association analysis of functional gene markers for provitamin A levels across diverse tropical yellow maize inbred lines. BMC Plant Biol. 2013;13(1):227-243. doi: 10.1186/1471–2229–13–227.
- Babu R, Rojas NP, Gao S, et al. Validation of the effects of molecular marker polymorphisms in LcyE and CrtRB1 on provitamin A concentrations for 26 tropical maize populations. Theor Appl Genet. 2013;126(2):389-399. doi: 10.1007/s00122–012–1987–3.
- Fraser PD, Bramley PM. The biosynthesis and nutritional uses of carotenoids. Progress in Lipid Research. 2004;43(3):228-265. doi: 10.1016/j.plipres.2003.10.002.
- Fu Z, Chai Y, Zhou Y, et al. Natural variation in the sequence of PSY1 and frequency of favorable polymorphisms among tropical and temperate maize germplasm. Theor Appl Genet. 2013;126(4):923-935. doi: 10.1007/s00122–012–2026–0.
- Fu ZY, Yan JB, Zheng YP, et al. Nucleotide diversity and molecular evolution of the PSY1 gene in Zea mays compared to some other grass species. Theor Appl Genet. 2010;120:709-720.
- Harjes CE, Rocheford TR, Bai L, et al. Natural Genetic Variation in Lycopene Epsilon Cyclase Tapped for Maize Biofortification. Science. 2008;319(5861):330-333. doi: 10.1126/science. 1150255.
- Krinsky NI, Johnson EJ. Carotenoid actions and their relation to health and disease. Mol Aspects Med. 2005;26(6):459-516. doi: 10.1016/j.mam.2005.10.001.
- Mishra P, Singh NK. Spectrophotometry and TLC based characterization of kernel carotenoids in short duration maize. Maydica. 2010;55:95-100.
- Owens BF, Lipka AE, Magallanes-Lundback M, et al. A foundation for provitamin A biofortification of maize: genome-wide association and genomic prediction models of carotenoid levels. Genetics. 2014;198:1699-1716.
- Safawo T, Senthil N, Raveendran M, et al. Exploitation of natural variability in maize for β-carotene content using HPLC and gene specific markers. Electronic Journal of Plant Breeding. 2010;1(4):548-555.
- Yang XH, Gao SB, Xu ST, et al. Characterization of a global germplasm collection and its potential utilization for analysis of complex quantitative traits in maize. Mol Breeding. 2011;28:511-526.
- Zhu, CF, Naqvi S, Breitenbach J, et al. Combinational genetic transformation generates a library of metabolic phenotypes for the carotenoid pathway in maize. Proceedings of the National Academy of Sciences. 2008;105(47):18232-18237.
Supplementary files














