Comparison of diagnostics of bacterial vaginosis according to clinical signs with results of laboratory investigations
- Authors: Shipitsina E.V.1, Khusnutdinova T.A.1, Ryzhkova O.S.1, Krysanova A.A.1, Budilovskaya O.V.1, Rybina E.V.1, Vorobyova N.E.1, Savicheva A.M.1, Gushchin A.E.2
-
Affiliations:
- D. O. Ott Research Institute of Obstetrics and Gynecology, RAMS
- Central Research Institute for Epidemiology
- Issue: Vol 65, No 4 (2016)
- Pages: 76-82
- Section: Articles
- Submitted: 15.09.2016
- Published: 15.09.2016
- URL: https://journals.eco-vector.com/jowd/article/view/5825
- DOI: https://doi.org/10.17816/JOWD65476-82
- ID: 5825
Cite item
Full Text
Abstract
Introduction. Bacterial vaginosis (BV) is associated with a number of reproductive health disorders, therefore timely and accurate diagnosis of this condition is exceedingly important.
Objective.Comparison of effectiveness of clinical and laboratory diagnostics of BV in women with vaginal discharge.
Material and methods. In total, 318 patients addressing gynecological clinics with complaints about vaginal discharge participated in the study. Clinical diagnostics of BV was performed in the clinics participating in patient enrollment in accordance with their clinical practice. For laboratory diagnostics, microscopy of Gram stained smears according to the Nugent method and quantitative real-time PCR were used. Sensitivity and specificity of clinical diagnostics of BV and the molecular method were evaluated using the Nugent method as reference standard.
Results. With the Nugent method, BV was diagnosed in 27% of women, with real-time PCR — in 37% of women. Using clinical signs of BV, the condition was diagnosed in 91% women. Sensitivity and specificity of the real-time PCR were 97% and 87%, respectively. Sensitivity of clinical diagnostics was 100%, but specificity was only 17%.
Conclusions. Diagnostics of BV based only on the presence of vaginal discharge leads to false positive results and requires laboratory confirmation. The molecular method has a high sensitivity and satisfactory specificity for BV diagnosis and can be used as an alternative to the Nugent method.
Full Text
Введение
Бактериальный вагиноз (БВ) — основная причина патологических выделений из влагалища у женщин репродуктивного возраста. БВ представляет собой нарушение нормального (физиологического) микробиоценоза влагалища, характеризующееся замещением нормальной лактобациллярной микрофлоры большим количеством анаэробных микроорганизмов. Исследования последних лет показывают, что БВ не только снижает качество жизни женщины, но и сопряжен с рядом воспалительных заболеваний органов мочеполового тракта и является одной из частых причин осложнений беременности [2–5]. Заболевание часто принимает рецидивирующую форму: у 60 % женщин наблюдаются рецидивы БВ в течение 12 месяцев после лечения [6]. Распространенность заболевания варьирует в исключительно широких пределах (7–68 %) в зависимости от региона, этнической/расовой принадлежности, обследуемой популяции, а также метода диагностики [1].
Диагностику БВ осуществляют с использованием ряда клинических и лабораторных методов. Основным методом клинической диагностики является метод Амселя [7], который предполагает использование 4 критериев: 1) наличие специфических выделений из влагалища (однородных, серовато-белых, жидких, c неприятным запахом); 2) pH отделяемого влагалища выше 4,5; 3) положительный аминный тест; 4) выявление «ключевых» клеток (отслоившихся клеток эпителия влагалища, поверхность которых усеяна бактериями, за счет чего они имеют «зернистый» вид) при микроскопическом исследовании нативного препарата. Если выполняются как минимум 3 критерия, устанавливается диагноз БВ. К преимуществам метода Амселя относится возможность диагностировать БВ во время приема врача и сразу назначить терапию. Недостатками являются субъективность и отсутствие возможности для микроскопического исследования нативного препарата у большинства врачей.
Среди методов лабораторной диагностики БВ наиболее распространенным является метод Нуджента [8], который основан на определении трех бактериальных морфотипов: крупные грамположительные палочки (морфотип лактобациллы), небольшие грамотрицательные или грамвариабельные кокки и коккобациллы (морфотип Gardnerella и Bacteroides) и грамотрицательные или грамвариабельные изогнутые палочки (морфотип Mobiluncus). В зависимости от суммы баллов образцы расценивают как нормальная микрофлора (число баллов от 0 до 3), промежуточная микрофлора (число баллов от 4 до 6) и БВ (число баллов от 7 до 10). Преимуществами метода Нуджента являются относительно высокая чувствительность и специфичность, высокая степень стандартизации, что обеспечивает высокую воспроизводимость. К недостаткам относятся трудоемкость и существование промежуточного варианта микрофлоры влагалища.
В нашей стране методы Амселя и Нуджента практически не используются. В реальной клинической ситуации диагностика БВ чаще всего основывается на одном из критериев Амселя — наличии патологических выделений из влагалища. Критерии повышенного значения pH отделяемого влагалища и положительного аминного теста применяются очень редко. В лучшем случае врач дополнительно принимает во внимание отсутствие лактобацилл и присутствие ключевых клеток в окрашенном по Граму препарате отделяемого влагалища.
В последние годы молекулярные методы активно внедряются в диагностику БВ. Большинство предлагаемых молекулярных тестов для диагностики этого заболевания основаны на выявлении клинически значимых количеств бактерий, ассоциированных с БВ. Высокие чувствительность и специфичность (в среднем 96 и 92 % соответственно) были показаны для отечественного теста АмплиПрайм Флороценоз-Бактериальный вагиноз (Флороценоз-БВ), разработанного в ФБУН «ЦНИИ эпидемиологии Роспотребнадзора», в основе которого лежит определение соотношения концентраций лактобацилл (Lactobacillus spp.), Gardnerella vaginalis и Atopobium vaginae [9, 10].
Целью данного исследования было изучение достоверности диагностики БВ на основании наличия клинических признаков урогенитальной инфекции — патологических влагалищных выделений — в сравнении с лабораторными методами диагностики БВ — микроскопическим по Нудженту и молекулярно-биологическим — ПЦР в реальном времени.
Материалы и методы
В исследовании участвовали женщины репродуктивного возраста, обратившиеся в лечебные учреждения гинекологического профиля (главным образом, женские консультации) Санкт-Петербурга с жалобами на выделения из влагалища. Критериями исключения являлись беременность и применение антибактериальных препаратов в течение последних 4 недель. В направлении на исследование указывался возраст пациенток и диагноз.
Материалом для лабораторного исследования служило отделяемое влагалища, которое получали с помощью двух дакроновых тампонов. Содержимое одного тампона наносили на предметное стекло, окрашивали по Граму и исследовали с помощью метода Нуджента. Содержимое второго тампона помещали в пробирку с транспортной средой ТСМ (ФБУН «ЦНИИ эпидемиологии Роспотребнадзора», Москва) для диагностики БВ методом ПЦР в реальном времени. ДНК выделяли с помощью набора реагентов АмплиПрайм ДНК-сорб-АМ (ФБУН «ЦНИИ эпидемиологии Роспотребнадзора», Москва) в соответствии с инструкцией производителя. ПЦР-амплификацию, анализ продуктов ПЦР и интерпретацию результатов осуществляли с использованием теста Флороценоз-БВ в соответствии с инструкцией производителя. Клиническая диагностика БВ проводилась в учреждениях, участвующих в наборе пациенток, в соответствии с принятой в данных учреждениях практикой.
Результаты молекулярного (Флороценоз-БВ) и клинического подходов к диагностике БВ оценивали по отношению к результатам, полученным на основе метода Нуджента. При расчете чувствительности и специфичности использовались только пробы, для которых были получены однозначные результаты — присутствие или отсутствие БВ.
Результаты
Всего в исследование было включено 318 женщин в возрасте от 18 до 54 лет (средний возраст — 31 год). Сведения о клиническом диагнозе были получены только для 136 (43 %) женщин. Для остальных женщин запись в графе «Диагноз» отсутствовала. Образцы биоматериала от всех включенных в исследования женщин были протестированы с помощью метода Нуджента и теста Флороценоз-БВ. C использованием метода Нуджента БВ был выявлен у 86 женщин (27 %), у 56 (18 %) — промежуточная микрофлора, у 176 (55 %) — нормальная микрофлора влагалища. С применением теста Флороценоз-БВ 118 проб (37 %) были охарактеризованы как БВ, 15 (5 %) — промежуточная микрофлора, 37 (12 %) — дисбиоз неуточненной этиологии, 9 (3 %) — недостаточное для анализа количество бактерий, 139 (44 %) — отсутствие БВ (табл. 1).
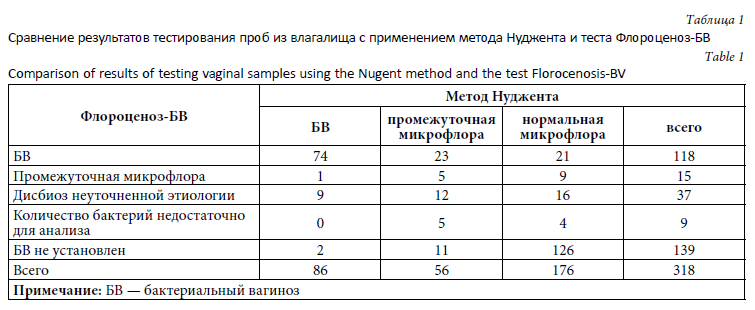
Из 86 случаев, определенных методом Нуджента как БВ, 74 были также охарактеризованы как БВ и с применением теста Флороценоз-БВ, 2 — как отрицательные на БВ, остальные — как промежуточная микрофлора (n = 1) и дисбиоз неуточненной этиологии (n = 9). Таким образом, чувствительность теста Флороценоз-БВ составила 97 % (табл. 2). В 126 из 176 случаев нормальной микрофлоры, установленных методом Нуджента, отсутствие БВ было также установлено с применением теста Флороценоз-БВ. В 21 случае нормальной микрофлоры по Нудженту тестом Флороценоз-БВ был выявлен БВ, остальные 29 случаев включали случаи промежуточной микрофлоры (n = 9), дисбиоза неуточненной этиологии (n = 16), недостаточного для анализа количества бактерий. В результате специфичность метода была оценена как 87 % (см. табл. 2).

У 124 из 136 женщин (91 %), имевших запись в графе «Диагноз», был диагностирован БВ (как единственный диагноз или в сочетании с другими заболеваниями). У оставшихся 12 женщин (9 %) были выявлены другие инфекционно-воспалительные заболевания урогенитального тракта, включающие вагинит, вульвовагинит, кандидозный вульвовагинит, цервицит (табл. 3).
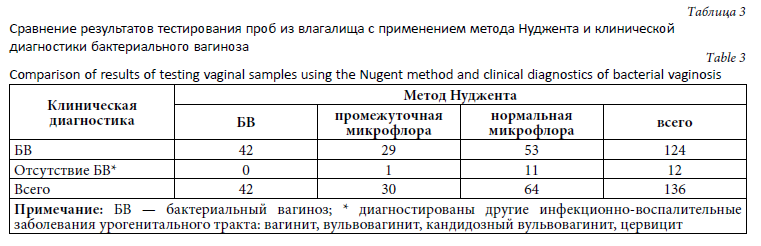
Все 42 случая БВ, выявленные методом Нуджента, были охарактеризованы как БВ и по клиническим признакам. Таким образом, чувствительность клинической диагностики равнялась 100 % (см. табл. 2). Однако из 64 случаев нормальной по методу Нуджента микрофлоры только 11 не имели клинического диагноза БВ, тогда как у 53 пациенток имевшаяся клиническая картина была неправильно классифицирована как БВ. В итоге специфичность клинического подхода составила всего 17 % (см. табл. 2).
Обсуждение результатов
Выделения из половых путей являются самой частой жалобой при обращении женщин к гинекологу, и одной из наиболее частых причин выделений является БВ. После проведенных лабораторных исследований мы установили распространенность БВ среди женщин с жалобами на выделения из влагалища, которая составила 27 %. Этот показатель находится в пределах описываемой в международной [11] и отечественной [9, 10] литературе частоты БВ в данной популяции женщин (20–30 %).
Кроме БВ, причинами патологических выделений из влагалища могут быть вагинит (кандидозный, трихомонадный, аэробный), а также цервицит. В недавнем исследовании при дифференциальной диагностике патологических влагалищных выделений распространенность БВ практически полностью совпала с результатами данного исследования и составила 27,4 % [12]. При этом другими заболеваниями, сопровождающимися выделениями из влагалища, были кандидозный вульвовагинит (выявлен у 30,7 % женщин, причем у 7,9 % в сочетании с БВ) и аэробный вагинит (диагностирован у 2,6 % женщин). В нашем исследовании из 136 женщин, для которых был указан диагноз, 124 был установлен диагноз БВ и только 12 — другие инфекционно-воспалительные заболевания урогенитального тракта. После проведения лабораторного исследования с использованием метода Нуджента диагноз БВ подтвердился только у 42 пациенток, у остальных 82 пациенток диагноз БВ был не обоснован. Несмотря на то что метод Нуджента во всем мире считается «золотым стандартом» диагностики БВ, в нашей стране в рутинной диагностике БВ практически не используется. Чаще всего диагностика БВ, особенно в условиях женской консультации, основывается только на одном из критериев Амселя — критерии выделений из влагалища, который обладает низкой специфичностью. Из других критериев Амселя наиболее специфичным для БВ критерием является обнаружение ключевых клеток, однако чувствительность этого критерия существенно варьирует — от 32 до 90 % [13–15]. Необходимо отметить, что, согласно классическому варианту метода Амселя, микроскопически исследуется нативный препарат, а не окрашенный по Граму, как это принято в нашей стране.
Молекулярные методы имеют ряд преимуществ перед другими методами диагностики БВ. К ним относятся в первую очередь объективная оценка результатов и высокий уровень стандартизации. Кроме того, в нашей стране, особенно в последние годы, молекулярные методы стали широко доступными и востребованными в диагностике целого ряда инфекционных болезней. Несмотря на то что в развитие БВ вовлечен широкий спектр бактерий, только ограниченный ряд микроорганизмов, а именно G. vaginalis, A. vaginae, Eggerthella, Prevotella, BVAB2, Megasphaera type 1,Leptotrichia/Sneathia, имеют потенциал для использования в качестве мишеней для диагностики БВ [16–19]. Связано это с тем, что эти виды присутствуют у большинства пациенток с БВ, что обеспечивает адекватную диагностическую чувствительность. Результаты многих работ свидетельствуют о том, что G. vaginalis и A. vaginae являются практически универсальными маркерами БВ, при этом использование количественных порогов существенно повышает специфичность тестов по выявлению этих микроорганизмов без значительного снижения чувствительности. Так, в работе J. Menard et al. [16] было показано, что определение количественного порога A. vaginae (108 копий/мл) и G. vaginalis (109 копий/мл) является точным методом диагностики БВ с чувствительностью 96 % и специфичностью 99 %. При определении содержания бактерий во влагалище женщин с БВ и без БВ методом пиросеквенирования было показано, что снижение содержания лактобацилл при одновременном увеличении содержания G. vaginalis и/или A. vaginae предсказывали БВ с чувствительностью 100 % и специфичностью 95 % [18].
В нашем исследовании тест Флороценоз-БВ показал высокую чувствительность для диагностики БВ (97 %). Однако его специфичность составила 87 % из-за того, что результаты исследования 21 образца с применением метода Нуджента были охарактеризованы как нормальная микрофлора, в то время как результаты ПЦР показали преобладание G. vaginalis и A. vaginae над лактобациллами. Необходимо отметить, что в 3 из этих проб концентрация лактобацилл была на 1–2 порядка ниже совокупной концентрации ДНК G. vaginalis и A. vaginae. Причинами несовпадения результатов ПЦР и метода Нуджента могут быть погрешности во взятии биологического материала. Пониженное количество бактерий на предметном стекле может приводить к искажению микроскопической картины и выдаваемого результата. При этом хорошо известно, что аналитическая чувствительность ПЦР значительно выше, чем у микроскопии, а лабораторное заключение в тесте Флороценоз-БВ строится на отношении концентрации G. vaginalis и A. vaginae к концентрации лактобацилл независимо от общего количества микроорганизмов, попавших в исследуемый образец. Другими словами, в данной ситуации можно говорить о более низкой по сравнению с ПЦР чувствительности метода Нуджента и о том, что метод Нуджента, как микроскопический метод, уступает в объективности методу количественной ПЦР.
Таким образом, у женщин с выделениями из влагалища, у которых на основании клинической картины диагностирован БВ, применение лабораторных методов позволяет подтвердить диагноз только примерно у трети из них. Молекулярный метод имеет высокую чувствительность и удовлетворительную специфичность для диагностики БВ и может использоваться в качестве альтернативного методу Нуджента подхода.
About the authors
Elena V. Shipitsina
D. O. Ott Research Institute of Obstetrics and Gynecology, RAMS
Author for correspondence.
Email: iagmail@ott.ru
PhD, Senior Researcher, Laboratory of Microbiology Russian Federation
Tatyana A. Khusnutdinova
D. O. Ott Research Institute of Obstetrics and Gynecology, RAMS
Email: iagmail@ott.ru
Researcher, Laboratory of Microbiology Russian Federation
Olga S. Ryzhkova
D. O. Ott Research Institute of Obstetrics and Gynecology, RAMS
Email: iagmail@ott.ru
Researcher, Laboratory of Microbiology Russian Federation
Anna A. Krysanova
D. O. Ott Research Institute of Obstetrics and Gynecology, RAMS
Email: iagmail@ott.ru
Researcher, Laboratory of Microbiology Russian Federation
Olga V. Budilovskaya
D. O. Ott Research Institute of Obstetrics and Gynecology, RAMS
Email: iagmail@ott.ru
Researcher, Laboratory of Microbiology Russian Federation
Elena V. Rybina
D. O. Ott Research Institute of Obstetrics and Gynecology, RAMS
Email: iagmail@ott.ru
Bacteriologist, Laboratory of Microbiology Russian Federation
Nadezhda E. Vorobyova
D. O. Ott Research Institute of Obstetrics and Gynecology, RAMS
Email: iagmail@ott.ru
PhD, MD, Researcher, Department of Endocrinology of Reproduction Russian Federation
Alevtina M. Savicheva
D. O. Ott Research Institute of Obstetrics and Gynecology, RAMS
Email: savitcheva@mail.ru
MD, Professor, Head of Laboratory of Microbiology Russian Federation
Alexander E. Gushchin
Central Research Institute for Epidemiology
Email: aguschn@pcr.ru
PhD, Head of the Laboratory for Molecular Diagnostic and Epidemiology of Reproductive Tract Infections Russian Federation
References
- Kenyon C, Colebunders R, Crucitti T. The global epidemiology of bacterial vaginosis: a systematic review. Am J Obstet Gynecol. 2013;209(6):505-523. doi: 10.1016/j.ajog.2013.05.006.
- Allsworth JE, Peipert JF. Severity of bacterial vaginosis and the risk of sexually transmitted infection. Am J Obstet Gynecol. 2011;205(2):113.e1-6. doi: 10.1016/j.ajog.2011.02.060.
- Taylor BD, Darville T, Haggerty CL. Does bacterial vaginosis cause pelvic inflammatory disease. Sex Transm Dis. 2013;40(2):117-122. doi: 10.1097/OLQ.0b013e31827c5a5b.
- Donati L, Di Vico A, Nucci M, et al. Vaginal microbial flora and outcome of pregnancy. Arch Gynecol ¬Obstet. 2010;281(4):589-600. doi: 10.1007/s00404-009-1318-3.
- Haggerty CL, Totten PA, Tang G, et al. Identification of novel microbes associated with pelvic inflammatory disease and infertility. Sex Transm Infect. 2016. pii: sextrans-2015-052285. doi: 10.1136/sextrans-2015-052285.
- Bradshaw CS, Morton AN, Hocking J, et al. High recurrence rates of bacterial vaginosis over the course of 12 months after oral metronidazole therapy and factors associated with recurrence. J Infect Dis.2006; 193:1478-1486. doi: 10.1086/503780.
- Amsel R, Totten PA, Spiegel CA, et al. Nonspecific vaginitis. Diagnostic criteria and microbial and epidemiologic associations. Am J Med. 1983;74:14-22.
- Nugent RP, Krohn MA, Hillier SL. Reliability of diagnosing bacterial vaginosis is improved by a standardized method of gram stain interpretation. J Clin Microbiol. 1991;29:297-301.
- Шалепо К.В., Назарова В.В., Менухова Ю.Н., и др. Оценка современных методов лабораторной диагностики бактериального вагиноза // Журнал акушерства и женских болезней. — 2014. — Т. LXIII. — № 1. — С. 26–32. [Shalepo KV, Nazarova VV, Menuhova JN, et al. Assessment of current methods of laboratory diagnosis of bacterial vaginosis. Journal of Obstetrics and Women’s Diseases. 2014; 63(1):26-32.
- (In Russ.).]
- Rumyantseva TA, Bellen G, Romanuk TN, et al. Utility of microscopic techniques and quantitative real-time polymerase chain reaction for the diagnosis of vaginal microflora alterations. J Low Genit Tract Dis. 2015;19 (2):124-8. doi: 10.1097/LGT.0000000000000060.
- Bautista CT, Wurapa E, Sateren WB, et al. Bacterial vaginosis: a synthesis of the literature on etiology, prevalence, risk factors, and relationship with chlamydia and gonorrhea infections. Mil Med Res.2016; 3:4. doi: 10.1186/s40779–016–0074–5.
- Румянцева Т.А., Сурсяков В.А., Хайруллина Г.А., и др. Вагинальные выделения у пациенток гинекологического профиля: этиология и подходы к диагностике // Акушерство и гинекология. — 2015. — № 8. — С. 96–101.
- [Rumyantseva TA, Sursyakov VA, Khairullina GA, et al. Vaginal discharge in gynecological patients: Etiology and approaches to diagnosis. Akusherstvo i Ginekologiya. 2015;8:96-101. (In Russ.).]
- Modak T, Arora P, Agnes C, et al. Diagnosis of bacterial vaginosis in cases of abnormal vaginal discharge: comparison of clinical and microbiological criteria. J Infect Dev Ctries. 2011;5(5):353-360.
- Mengistie Z, Woldeamanuel Y, Asrat D, Yigeremu M. Comparison of clinical and gram stain diagnosis methods of bacterial vaginosis among pregnant women in Ethiopia. J Clin Diagn Res. 2013;7(12):2701-2703. doi: 10.7860/JCDR/2013/5872.3736.
- Sha BE, Chen HY, Wang QJ, et al. Utility of Amsel criteria, Nugent score, and quantitative PCR for Gardnerella vaginalis, Mycoplasma hominis, and Lactobacillus spp. for diagnosis of bacterial vaginosis in human immunodeficien¬cy virus-infected women. J Clin Microbiol. 2005;43(9):
- -12. doi: 10.1128/JCM.43.9.4607-4612.2005.
- Menard JP, Mazouni C, Fenollar F, et al. Diagnostic accuracy of quantitative real-time PCR assay versus clinical and Gram stain identification of bacterial vaginosis. Eur J Clin Microbiol Infect Dis. 2010;29(12): 1547-52. doi: 10.1007/s10096-010-1039-3.
- Cartwright CP, Lembke BD, Ramachandran K, et al. Development and validation of a semi-quantitative, multi-target, PCR assay for the diagnosis of bacterial vaginosis. J Clin Microbiol. 2012;50:2321-2329. doi: 10.1128/JCM.00506-12.
- Shipitsyna E, Roos A, Datcu R, et al. Composition of the vaginal microbiota in women of reproductive age - sensitive and specific molecular diagnosis of bacterial vaginosis is possible? PLoS One.2013;8(4):e60670. doi: 10.1371/journal.pone.0060670.
- Fredricks DN, Fiedler TL, Thomas KK, et al. Targeted PCR for detection of vaginal bacteria associated with bacterial vaginosis. J Clin Microbiol. 2007;45:3270-3276. doi: 10.1128/JCM.01272-07.
Supplementary files







